郑州源创基因科技有限公司成立于2016年,由哥伦比亚大学博士后赵辉,归国创办的国家高新技术企业。拥有97项知识产权及实用技术,业务遍布上海、重庆、深圳、北京等城市,总部在郑州航空港区。
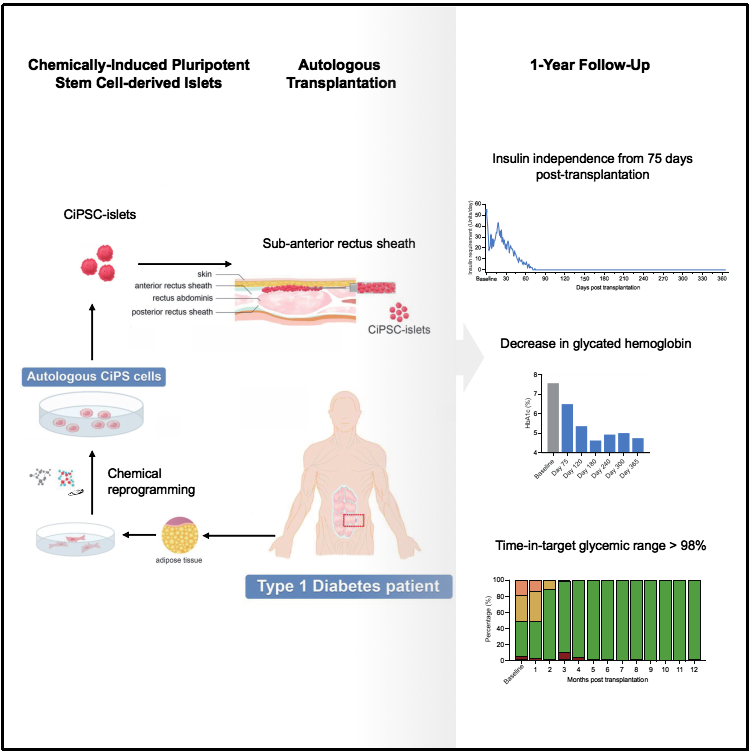
国际权威期刊《CELL》刊载了一项由中国科学家团队完成的重大研究:首次通过基于干细胞的疗法,成功实现1型糖尿病患者的临床功能性治愈。研究论文题为《Transplantation of Chemically Induced Pluripotent Stem-Cell-Derived Islet Under Abdominal Anterior Rectus Sheath in a Type 1 Diabetes Patient》。

这一突破性成果,不仅为全球数亿糖尿病患者带来了新希望,更标志着再生医学在重大疾病治疗领域迈入了新纪元。
1型糖尿病
糖尿病是一种以长期高血糖为特征的代谢性疾病,主要分为1型、2型和妊娠期糖尿病。据国际糖尿病联盟(IDF)2021年报告,全球糖尿病患者约5.37亿人。
2型糖尿病最为常见,约占患者总数的90%-95%;1型糖尿病占比约5%-10%。尽管比例较低,但1型糖尿病多发生于儿童和青少年,对患者生活质量和长期健康影响显著。因其自身免疫性发病机制特殊、治疗难度大,一直是医学研究的重点。
1型糖尿病的本质是自身免疫性疾病,患者自身的免疫系统错误地攻击并破坏胰腺中负责分泌胰岛素的β细胞,导致胰岛素绝对缺乏。胰岛素是调节血糖的关键激素,其缺失导致血糖失控,引发一系列严重并发症。
在1型糖尿病的发病过程中,胰腺胰岛β细胞成为免疫攻击的主要靶点。具体机制涉及多种免疫细胞(如树突状细胞、T细胞)对β细胞特异性抗原的识别与反应,最终导致功能性β细胞大量丧失和胰岛素分泌严重不足。
传统治疗方法
长期以来,1型糖尿病的治疗主要依赖外源胰岛素注射,但这种方式存在明显局限:
血糖控制难以精准模拟健康胰腺的生理调节。
患者需终身依赖胰岛素,严重影响生活质量。
长期血糖控制不佳易导致心血管疾病、肾病、视网膜病变等严重并发症。
胰岛素使用不当可能引发危及生命的低血糖事件。
干细胞疗法
干细胞因其自我更新和分化潜能成为医学研究热点,主要分为三类:
胚胎干细胞 (ESCs): 来源于早期胚胎,具有分化为所有细胞类型的全能性,但临床应用受伦理限制。
成体干细胞: 存在于骨髓、脂肪等组织中,分化潜能有限,主要用于特定组织修复。
诱导多能干细胞 (iPSCs): 通过引入特定因子(遗传或化学方法),将成熟体细胞(如皮肤细胞)重编程为具有类似胚胎干细胞多能性的细胞。该技术规避了胚胎干细胞的伦理问题,并支持个体化治疗。
在1型糖尿病治疗领域,科学家致力于将诱导多能干细胞定向分化为功能性胰岛细胞(包含β细胞),以替代患者体内受损的胰岛组织,这是突破当前治疗瓶颈的关键策略。

突破性研究:从实验室到临床
此项研究采用了创新的化学重编程技术,利用特定化学小分子组合将成熟体细胞直接诱导为多能干细胞(化学诱导多能干细胞, CiPSCs),无需传统的基因操作。该技术因其安全性和高效性备受关注,并于2024年荣获未来科学大奖“生命科学奖”。
在前期非人灵长类动物实验中,该疗法已展现良好的有效性和安全性。经部门批准后,研究团队对一名病史11年、长期依赖胰岛素但血糖控制不佳、频发严重低血糖的1型糖尿病患者进行了临床试验。
治疗过程包含三个核心步骤:
利用化学重编程技术将患者自身体细胞转化为CiPSCs。
将CiPSCs定向高效分化为具有胰岛素分泌功能的人胰岛细胞。
将体外培养的功能性人胰岛细胞移植回患者体内。
结果显示,移植后75天,患者完全停用外源胰岛素,且该状态已稳定维持超过一年。更关键的是,患者的多项糖尿病关键指标均恢复至正常水平,实现了1型糖尿病的临床功能性治愈。这标志着干细胞疗法在该领域取得了重大突破。
干细胞疗法的临床应用优势
相较于传统疗法,干细胞疗法优势显著:
更精细的血糖调节:干细胞衍生的胰岛细胞有望更接近生理性地调节血糖,提升疗效,降低并发症风险。
长期疗效潜力:可能实现长期甚至永久性缓解,极大改善患者生活质量。
个体化治疗:利用患者自身细胞制备CiPSCs和胰岛细胞,可显著降低免疫排斥风险,实现“量身定制”。

展望
尽管初步成果令人鼓舞,但该技术走向广泛应用仍需开展更大规模、更长期的临床研究,以全面评估安全性和持久疗效。
中国科学家在1型糖尿病治疗领域的这一突破,不仅为该疾病带来了革命性的治疗前景,也为再生医学应用于其他难治性疾病提供了重要范例。随着研究的深入和技术的迭代,干细胞疗法有望改变1型糖尿病的治疗格局,为人类健康事业开辟新的篇章。
https://pubmed.ncbi.nlm.nih.gov/39326417/
https://mp.weixin.qq.com/s/a2ynx9ABWd0VQQfBV61znw