郑州源创基因科技有限公司成立于2016年,由哥伦比亚大学博士后赵辉,归国创办的国家高新技术企业。拥有97项知识产权及实用技术,业务遍布上海、重庆、深圳、北京等城市,总部在郑州航空港区。
2025年7月29日,国际顶尖期刊《Signal Transduction and Targeted Therapy》(STTT)在线发表了一项开创性研究,为深陷治疗困境的失代偿性肝硬化(DLC)患者带来了新的曙光。

这项由中国人民解放军总医院第五医学中心、国家感染性疾病临床研究中心王福生院士领衔的团队完成的I期临床试验,首次系统性地在人体内探索了间充质干细胞(MSC)治疗DLC的安全剂量、关键作用机制,为寻找肝移植之外的有效疗法迈出了关键一步。
失代偿性肝硬化的困境与干细胞潜力
失代偿性肝硬化(DLC)是肝硬化进展的严重阶段。此时,患者不仅面临严重的肝功能衰竭,还伴随着复杂的免疫失调——表现为一种矛盾状态:全身炎症反应过度活跃的同时,机体抵抗感染的能力却显著下降,导致患者极易发生感染,病情迅速恶化。
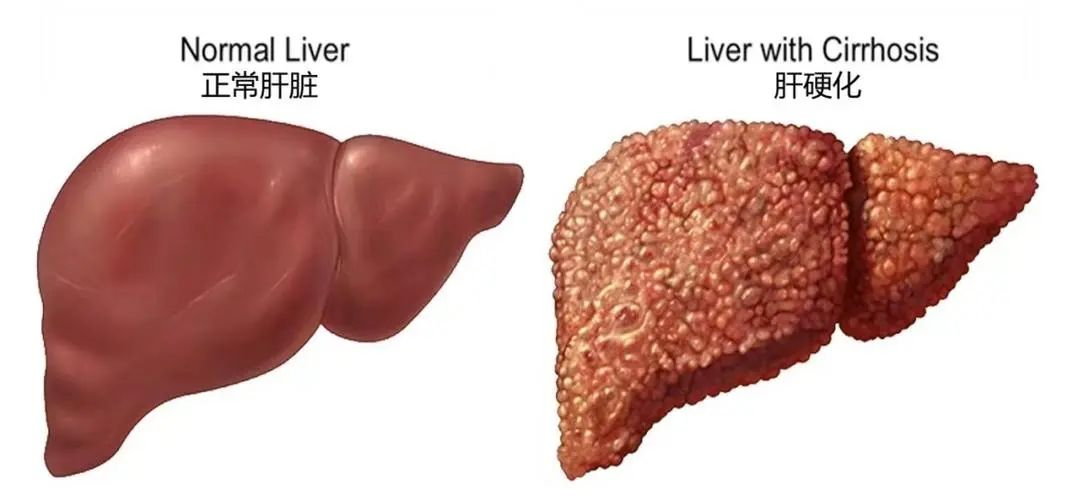
目前,肝移植是唯一能根治DLC的方法。然而,供体肝脏严重短缺、手术风险高以及费用昂贵,使得绝大多数患者难以获得移植机会。据国内研究数据估算,我国现有肝硬化患者约700万-800万人,其中处于失代偿期的患者数量达百万级别,治疗需求巨大。
间充质干细胞(MSC)因其强大的免疫调节和组织修复潜能,被视为治疗DLC的潜在希望。既往研究表明,MSC可能通过平衡免疫反应、促进损伤修复来改善肝硬化症状。然而,MSC治疗DLC的最佳剂量、给药方式以及在人体内的确切作用机制尚不清楚,这严重阻碍了其临床应用。为了填补这一空白,王福生院士团队精心设计了这项剂量递增的I期临床试验。
研究设计:系统探索安全剂量
研究分为两个阶段,共纳入24名中位年龄51岁的中重度DLC患者(Child-Pugh评分中位数8.12分),病因主要为乙肝病毒和酒精。
Ia期(单剂量试验):采用“3+3”剂量递增设计。4组患者分别单次输注不同剂量MSC(5.0×10⁷至2.0×10⁸细胞)。治疗后密切随访28天,并运用单细胞RNA测序等先进技术分析免疫细胞动态变化。
Ib期(多剂量试验):基于Ia期结果,选取两个剂量组(1.0×10⁸和2.0×10⁸细胞/次),患者每周接受1次输注,共3次,随访至28天,评估多剂量方案的安全可行性。
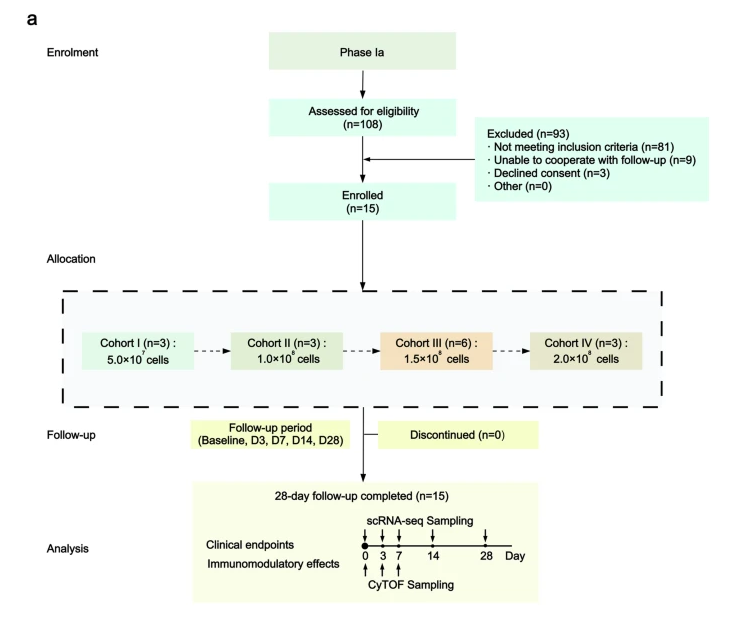
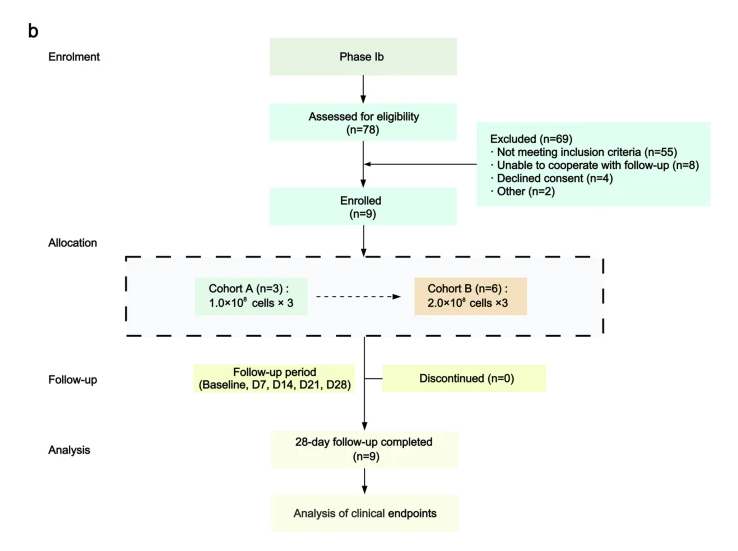
关键发现:安全可控、机制明朗、疗效初显
经过28天的严密监测,该研究取得了多项突破性进展:
安全可靠:所有患者(包括单次高剂量和多次给药)均未发生严重不良事件或剂量限制性毒性。仅报告少数轻微反应(如短暂皮疹、低热),程度轻且与MSC输注相关性低。这为后续研究提供了坚实的安全基础。
机制明朗:研究发现MSC的免疫调节效果具有剂量依赖性——高剂量组(尤其是2.0×10⁸细胞)效果更显著。研究首次在人体内锁定关键作用靶点:MX1+ 单核细胞。
这类细胞在DLC患者体内异常增多且高度活跃(促炎)。
MSC输注后,尤其在高剂量下,能显著减少MX1+单核细胞数量并抑制其功能活性。
这种有益变化在治疗后第7天达峰,14天后减弱,提示未来需优化给药间隔以维持效果。

疗效初显:尽管主要评估安全性,但也观察到积极的临床改善信号,且在高剂量与多剂量组更明显:
肝功能:白蛋白、胆碱酯酶等合成功能指标有提升趋势;Child-Pugh和MELD等关键评分观察到下降趋势。
生活质量:多剂量组患者的慢性肝病问卷(CLDQ)评分显示改善趋势(报告改善率88.9%),提示症状(如疲劳、腹胀)可能缓解。
意义与展望
这项开创性的I期临床试验意义重大,首先证实了MSC治疗失代偿性肝硬化在选定剂量方案下的安全性;且首次在人体内系统阐明了MSC的剂量效应关系,并揭示了其通过抑制过度活跃的MX1+单核细胞来调节免疫的关键作用机制,识别了潜在的疗效生物标志物。

这些发现如同绘制了一张精准的“治疗导航图”,为未来优化MSC治疗方案(如最佳剂量、频次)和实现个体化精准治疗奠定了科学基石。虽然仍需更大规模试验验证长期疗效和确定最终方案,但对于数百万DLC患者而言,这项研究无疑点亮了一盏充满希望的明灯。
间充质干细胞疗法正加速从实验室的“潜在可能”迈向临床应用的“现实希望”。未来,它有望成为肝移植的有力补充,为终末期肝病患者提供一条更可及、更安全的生命新通道。
https://mp.weixin.qq.com/s/6k5y5wMRcsLeGxWuqnGblw
https://www.nature.com/articles/s41392-025-02318-4